7 Marzo, 2019
Una collaborazione tra l’Istituto di Ricerca in Biomedicina (IRB), affiliato all’Università della Svizzera italiana (USI), l’Institute for Protein Design, Washington University, USA, il Center for Molecular Medicine, Karolinska Institutet, Stoccolma, Svezia ed il Fred Hutchinson Cancer Research Center, Seattle, USA, fornisce una nuova speranza per lo sviluppo di un vaccino contro il virus respiratorio sinciziale umano (hRSV). La ricerca è stata pubblicata oggi nella prestigiosa rivista scientifica Cell.
Introduzione
Il virus respiratorio sinciziale umano (hRSV) è considerato una minaccia in ambito sanitario mondiale. Quale causa di mortalità infantile, esso risulta essere secondo solo alla malaria. L’infezione di adulti in salute provoca tipicamente tenui sintomi respiratori. Al contrario, essa può risultare molto pericolosa nei bambini e negli anziani ed è responsabile di un considerevole tasso di ospedalizzazione in entrambi i gruppi per quanto riguarda i paesi industrializzati.
Sulla superficie di hRSV si trovano tre proteine: F, G e SH. La prima consente la fusione tra la membrana del virus e quella delle cellule umane ospiti.
Numerosi studi hanno dimostrato che il siero di persone infettate è in grado di neutralizzare il virus grazie alla presenza di anticorpi indirizzati per la maggior parte contro la proteina F. Per questo motivo, molti degli sforzi impiegati nella ricerca di un vaccino sono focalizzati su quest’ultima. Ciononostante, nessun vaccino si è ancora dimostrato efficace contro hRSV. Questo può essere spiegato della natura stessa delle proteine virali di fusione. Esse subiscono infatti importanti riarrangiamenti strutturali aventi luogo nella fase di transizione che le porta da uno stadio definito di prefusione, precedente l’infezione, ad uno di postfusione che si realizza al momento dell’infezione della cellula ospite. I potenziali vaccini proposti finora comprendevano la proteina F in postfusione. In fasi cliniche, questi ultimi hanno però indotto solo lievi aumenti nel titolo di anticorpi neutralizzanti.
La scoperta
Il nostro studio descrive lo sviluppo di nanoparticelle proteiche in grado di auto-assemblarsi ed esporre sulla loro superficie una variante stabilizzata della proteina virale di fusione F. Questo potenziale vaccino è in grado di indurre una risposta anticorpale con attività neutralizzante che si è dimostrata essere all’incirca dieci volte superiore rispetto a quella promossa da altri vaccini attualmente impiegati in fasi di ricerca clinica.
 |
|
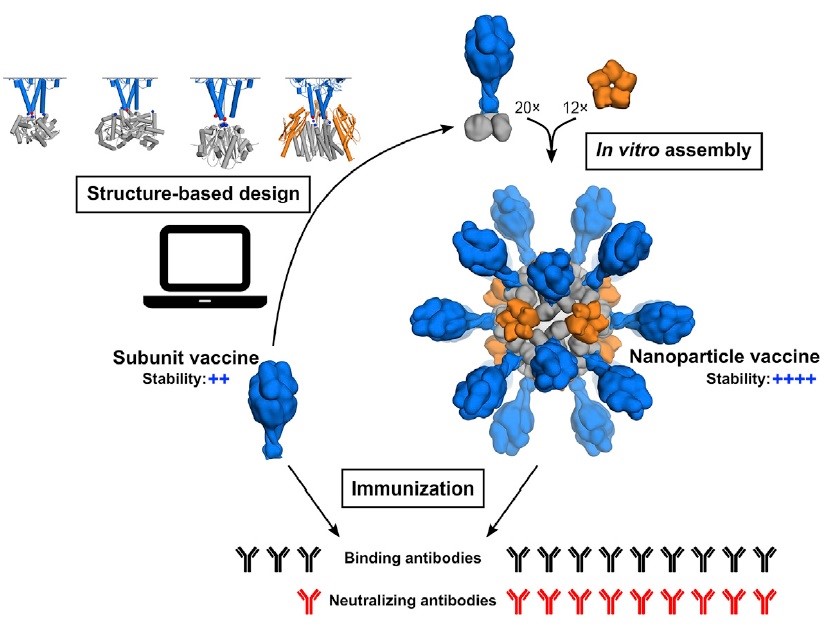
Illustrazione rappresentante una nanoparticella a partire dalla sua creazione al computer fino all’auto-assemblaggio avente luogo in vitro. Ogni nanoparticella, che espone sulla sua superficie 20 copie della proteina virale di fusione F, è in grado di indurre una potente risposta anticorpale neutralizzante. |
La nostra ricerca porta nuova speranza per lo sviluppo di un efficace vaccino contro il virus respiratorio sinciziale umano. Inoltre, corrobora l’utilizzo di nanoparticelle quale strumento per lo sviluppo di vaccini contro altre malattie infettive. Questa valida soluzione risulta essere di particolare importanza nei casi in cui l’antigene di interesse sia poco stabile o poco immunogenico.
Lo studio è stato coordinato da Laurent Perez presso l’Istituto di Ricerca in Biomedicina di Bellinzona (IRB, affiliato all’USI) e Neil P. King presso l’Insitute for Protein Design, Dipartimento di Biochimica, Washington University, negli Stati Uniti. Inoltre, esso ha coinvolto anche il Center for Molecular Medicine, Karolinska Institutet, in Svezia ed il Fred Hutchinson Cancer Research Center a Seattle negli Stati Uniti.
Il lavoro nel suo insieme, è stato reso possibile grazie a fondi concessi dalla Fondazione Bill e Melinda Gates.
L’importanza di questo studio è stato riconosciuto da Rino Rappuoli, immunologo di fama mondiale che attualmente riveste la carica di direttore scientifico e responsabile dell’attività di ricerca e sviluppo esterna presso GlaxoSmithKline (GSK) Vaccines. Il suo commento si trova nella medesima edizione di Cell dell’articolo.
Articolo:
Jessica Marcandalli, Brooke Fiala, Sebastian Ols, Michela Perotti, Willem de van der Schueren, Joost Snijder, Edgar Hodge, Mark Benhaim, Rashmi Ravichandran, Lauren Carter, Will Sheffler, Livia Brunner, Maria Lawrenz, Patrice Dubois, Antonio Lanzavecchia, Federica Sallusto, Kelly K. Lee, David Veesler, Colin E. Correnti, Lance J. Stewart, David Baker, Karin Loré, Laurent Perez, Neil P. King. Cell.
J. Marcandalli and B. Fiala contributed equally to this work. L. Perez and N. P. King contributed equally to this work and are co-corresponding authors.